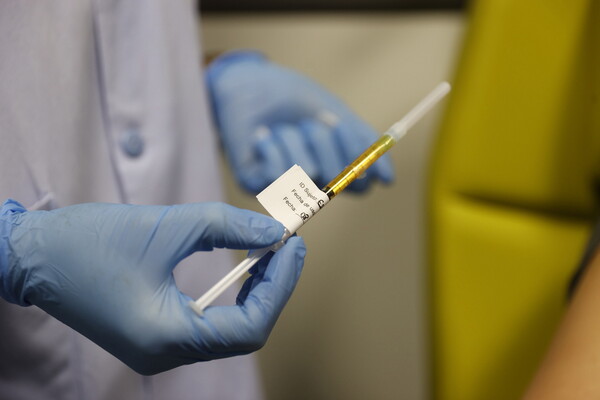
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ) ανακοίνωσε ότι ξεκίνησε την «κυλιόμενη αξιολόγηση» του εμβολίου της CureVac για τον κορωνοϊό.
Πρόκειται για το πρώτο βήμα της διαδικασίας για την επίσημη κατάθεση αίτησης για την έγκριση του εμβολίου στην Ευρωπαϊκή Ένωση.
Η απόφαση «βασίζεται στα προκαταρκτικά αποτελέσματα εργαστηριακών μελετών (μη κλινικά δεδομένα) και προκαταρκτικών κλινικών δοκιμών σε ενήλικες», αναφέρει στην ανακοίνωσή του ο Οργανισμός.
«Η κυλιόμενη αξιολόγηση θα πραγματοποιείται μέχρι να είναι διαθέσιμα επαρκή στοιχεία για την κατάθεση επίσημης αίτησης για άδεια κυκλοφορίας στην αγορά», διευκρινίζει ο ΕΜΑ και σημειώνει ότι θα αξιολογήσει τα δεδομένα άλλων κλινικών δοκιμών, μόλις αυτά είναι διαθέσιμα.
Το εμβόλιο της CureVac για τον κορωνοϊό βασίζεται στην τεχνολογία του mRNA και θα παραχθεί από τη Bayer, ενώ βρίσκεται στη φάση ΙΙΙ των κλινικών δοκιμών. Αν όλα πάνε καλά, η αίτηση στον ΕΜΑ μπορεί να γίνει τον Απρίλιο, δήλωσε ο Πέτερ Κρέμσνερ, ο καθηγητής του Ινστιτούτου του Τούμπινγκεν ο οποίος εποπτεύει τις κλινικές δοκιμές.
Από την πλευρά του, ο ΕΜΑ επιφυλάχθηκε για το χρονοδιάγραμμα, σημειώνοντας ότι δεν μπορεί να κάνει προβλέψεις, παρότι η διαδικασία διευκολύνεται από την κυλιόμενη αξιολόγηση. Αυτή η διαδικασία επιτρέπει στον Οργανισμό να εξετάζει τα δεδομένα για την ασφάλεια και την αποτελεσματικότητα των εμβολίων άμα τη εμφανίσει τους, πριν από την επίσημη κατάθεση αίτησης για έγκριση από τον κατασκευαστή. Στόχος είναι με αυτό τον τρόπο να επιταχύνεται η αξιολόγηση της αίτησης.
Άλλα δύο εμβόλια βρίσκονται σε διαδικασία «κυλιόμενης αξιολόγησης» από τον ΕΜΑ. Πρόκειται για εκείνα των εταιρειών Johnson & Johnson και Novavax. Έως τώρα, ο Ευρωπαϊκός Οργανισμός Φαρμάκων έχει δώσει το «πράσινο φως» σε τρία εμβόλια για τον κορωνοϊό. Πρόκειται για αυτό που ανέπτυξαν οι εταιρείες Pfizer και BioNTech, το εμβόλιο της Moderna και εκείνο που ανέπτυξε η AstraZeneca σε συνεργασία με το πανεπιστήμιο της Οξφόρδης.
Με πληροφορίες από ΑΠΕ/ ΑFP